Catalisador é toda e qualquer substância que acelera uma reação, diminuindo a energia de ativação e a energia do complexo ativado, sem ser consumido durante o processo. Um catalisador normalmente promove um caminho (mecanismo) molecular diferente para a reação. Por exemplo, hidrogênio e oxigênio gasosos são virtualmente inertes à temperatura ambiente, mas reagem rapidamente quando expostos à platina, que, por sua vez, é o catalisador da reação.
A sequência a seguir mostra as etapas de uma reação em que há atuação de um catalisador:
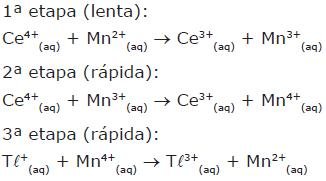
- cat.JPG (15.11 KiB) Exibido 2573 vezes
Considerando o processo global e as suas três etapas, pode-se dizer que a espécie que atua como catalisador é
A)
[tex3]Ce ^{4+}[/tex3].
B)
[tex3]Ce ^{3+}[/tex3].
C)
[tex3]Mn ^{2+}[/tex3].
D)
[tex3]Mn ^{3+}[/tex3].
E)
[tex3]Tl ^+[/tex3].
Alguém pode me falar como identificar o catalisador nessas reações, por gentileza??
Geralmente, eu encontro o catalisador quando ele não é consumido na reação, ou seja, aparece em ambos os lados, mas esse me parece diferente...
![🔴 [ENEM 2025 PPL Live 06] Matemática - Resolução de 161 até 165](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/ucQZ6Qn91JM/mqdefault.jpg)
![🔴 [ENEM 2025 PPL Live 05] Matemática - Resolução de 156 até 160](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/m2T1rBKy2qU/mqdefault.jpg)
![🔴 [ENEM 2025 PPL Live 04] Matemática - Resolução de 151 até 155](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/1scCX1e_dZo/mqdefault.jpg)
![🔴 [ENEM 2025 PPL Live 03] Matemática - Resolução de 146 até 150](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/fD8ohgS6JKo/mqdefault.jpg)
![🔴 [ENEM 2025 PPL Live 02] Matemática - Resolução de 141 até 145](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/np7jAEKAjTE/mqdefault.jpg)
![🔴 [ENEM 2025 PPL Live 01] Matemática - Resolução de 136 até 140](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/vb1b6e7VXjw/mqdefault.jpg)

