Olá
leonardodlc,
O boro do BF3 tem um orbital 2p vazio que pode acomodar um par de elétrons e atuar como ácido de lewis.
Já o HCN possui um hidrogênio polarizado com carga parcial positiva, ou seja, possui uma nuvem eletrônica deficiente em elétrons e pode receber um par de elétrons da amônia, por exemplo, atuando como base de lewis. Observe as imagens:
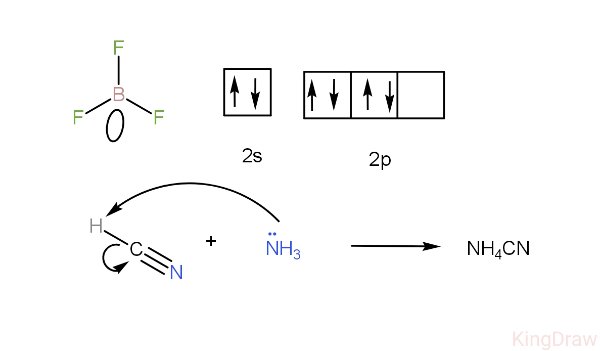
- KingDraw200608115054(1)(1).JPEG (12.42 KiB) Exibido 2309 vezes

