Página 1 de 1
(Covest - 2007) Termoquímica
Enviado: 12 Set 2012, 17:58
por felps
Alguém poderia me ajudar?
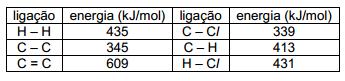
Utilize as energias de ligação da Tabela abaixo para calcular o valor absoluto do
[tex3]\Delta H[/tex3] de formação
(em
[tex3]kJ/mol[/tex3]) do cloro-etano a partir de eteno e do
[tex3]HCl[/tex3].
- imagem.JPG (9.77 KiB) Exibido 8086 vezes
Re: (Covest-2007) Termoquímica
Enviado: 12 Set 2012, 18:45
por theblackmamba
Reação de adição (hidro-halogenação):
[tex3]C_2H_4+HC\ell \rightarrow C_2H_5C\ell[/tex3]
[tex3]\begin{cases}C_2H_4\,\,\Rightarrow \,\,1\text{C=C}\,;\,\,\,4\text{C---H} \\ C_2H_5C\ell \,\,\Rightarrow \,\,1\text{C---C}\,;\,\,\,4\text{C---H}\,;\,\,\,1\text{C---Cl} \end{cases}[/tex3]
Para a energia de formação devemos fazer (não sei porque devemos utilizar o sinal negativo, mas dá certo)
[tex3]-\Delta H=H_{prod}-H_{reag}[/tex3]
[tex3]-\Delta H=[\cancel{(5\cdot 413)}+(1\cdot 345)+(1\cdot 339)]-[(1\cdot 431)+\cancel{(4\cdot 413)}+(1\cdot 609)][/tex3]
[tex3]-\Delta H=413+345+339-431-609[/tex3]
[tex3]\Delta H=-57\,\text{kJ}[/tex3]
Como enunciado pede o valor absoluto por mol de cloroetano temos que fazer:
[tex3]|\Delta H|=\frac{57}{1}[/tex3]
[tex3]\boxed{\Delta H=57\,\text{kJ/mol}}[/tex3]