Página 1 de 1
(Medicina Facisb 2017) pH e pOH
Enviado: 09 Mar 2017, 08:07
por Liliana
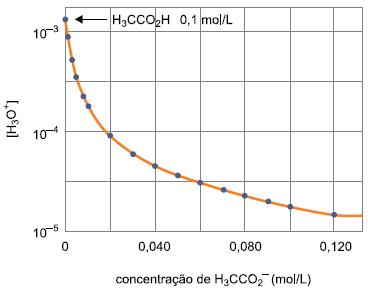
O gráfico mostra o efeito da adição de acetato de sódio a uma solução aquosa de ácido acético [
[tex3]H_3CCO_2H[/tex3] (aq)] na concentração de 0,1 mol/L, a 25 ºC.
- phpoh.JPG (14.63 KiB) Exibido 2169 vezes
Para obter uma solução final cujo pH seja 4,7, a concentração de acetato de sódio no sistema deve ser próxima de
(A) 0,060.
(B) 0,100.
(C) 0,120.
(D) 0,050.
(E) 0,035.
Re: (Medicina Facisb 2017) pH e pOH
Enviado: 10 Mar 2017, 07:54
por VALDECIRTOZZI
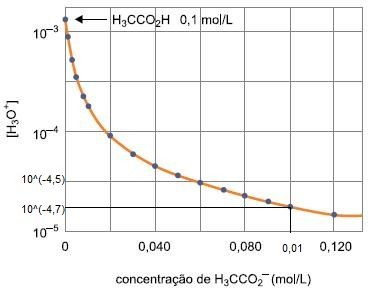
Se o [tex3]pH=4,7[/tex3], temos que [tex3]-\log \left[H^+\right]=4,7 \Longleftrightarrow \left[H^+\right]=10^{-4,7}[/tex3].
Observando o gráfico, vemos que esse valor é atingido (no eixo das ordenadas) quando o valor da concentração dos íon acetato está em torno de 0,01 mol/L.
Espero ter ajudado!
Re: (Medicina Facisb 2017) pH e pOH
Enviado: 10 Mar 2017, 10:41
por Liliana
Eu fiz assim
H3CCOOH + H3CCOONa -> H+ + Na+ + 2H3CCOO-
Considerando que em 10^-4,7 tem-se, aproximadamente, no eixo das abscissas, o valor 0,08 de H3CCO2- e que no início, a concentração de H3CCOO2H=0,1 mol/L= concentração de H3CCOONa, então
0,1 mol H3CCOONa - 0,2 mol H3CCOO-
x - 0,08
x=0,04 e seria a alternativa e) a mais próxima
Não estou entendendo :/
Re: (Medicina Facisb 2017) pH e pOH
Enviado: 10 Mar 2017, 14:32
por VALDECIRTOZZI
Observe o gráfico:
- gráfico.jpg (16.71 KiB) Exibido 2158 vezes
Re: (Medicina Facisb 2017) pH e pOH
Enviado: 10 Mar 2017, 19:25
por Liliana
A relação 2 H3CCOO2- : 1 H3CCOONa não é válida? Por que aí seria 0,1 de H3CCOO2- e então, 0,05 de H3CCOONa