A tabela abaixo apresenta dados de solubilidade, em gramas da substância por 100 g de água, na temperatura indicada. Em seguida, são apresentadas duas equações referentes ao comportamento em água das duas substâncias.
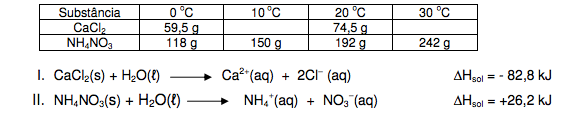
- Captura de Tela 2019-07-27 às 15.15.52.png (26.17 KiB) Exibido 1858 vezes
Com base nos dados da tabela e nas equações apresentadas pode-se afirmar,
(a) O processo de dissolução dos dois sais é endotérmico.
(b) A variação da solubilidade com a temperatura, não tem relação com o ∆Hsol.
(c) O aumento da temperatura desfavorece a dissolução do NH4NO3.
(d) O aumento da temperatura desfavorece a dissolução do CaCl2.
(e) A equação II representa a decomposição do sal
Por que a letra D está errada? Pensei que quando aumenta a temperatura a reação é deslocada para o sentido endotérmico. Então na II. a dissolução diminuiria.
![🔴 [ENEM 2025 PPL Live 06] Matemática - Resolução de 161 até 165](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/ucQZ6Qn91JM/mqdefault.jpg)
![🔴 [ENEM 2025 PPL Live 05] Matemática - Resolução de 156 até 160](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/m2T1rBKy2qU/mqdefault.jpg)
![🔴 [ENEM 2025 PPL Live 04] Matemática - Resolução de 151 até 155](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/1scCX1e_dZo/mqdefault.jpg)
![🔴 [ENEM 2025 PPL Live 03] Matemática - Resolução de 146 até 150](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/fD8ohgS6JKo/mqdefault.jpg)
![🔴 [ENEM 2025 PPL Live 02] Matemática - Resolução de 141 até 145](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/np7jAEKAjTE/mqdefault.jpg)
![🔴 [ENEM 2025 PPL Live 01] Matemática - Resolução de 136 até 140](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/vb1b6e7VXjw/mqdefault.jpg)

