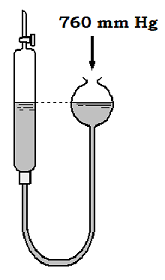
No início de uma experiência, a bureta do lado esquerdo da figura estava completamente cheia de água. Pela torneira da bureta, foi admitido nitrog~enio gasoso puro. Após a admissão do nitrogênio, o nível de água na bureta ficou na mesma altura que no recipiente do lado direito da figura. A pressão ambiente externa era 760mmHg e a temperatura era 25ºC. Nesta temperatura, a pressão de vapor da água é 24mmHg.
- 185.png (8.47 KiB) Exibido 1788 vezes
Assinale a afirmação falsa a respeito do volume gasoso dentro da bureta após o estabelecimento do equilíbrio.
a) 736/760 das moléculas correspondem a N2.
b) A pressão total é de 784mmHg
c) A pressão parcial do vapor de água é 24mmHg
d) A pressão parcial do nitrogênio é 736mmHg
e) A fração molar das moléculas de água é 24/760
![🔴 [ENEM 2025 PPL Live 06] Matemática - Resolução de 161 até 165](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/ucQZ6Qn91JM/mqdefault.jpg)
![🔴 [ENEM 2025 PPL Live 05] Matemática - Resolução de 156 até 160](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/m2T1rBKy2qU/mqdefault.jpg)
![🔴 [ENEM 2025 PPL Live 04] Matemática - Resolução de 151 até 155](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/1scCX1e_dZo/mqdefault.jpg)
![🔴 [ENEM 2025 PPL Live 03] Matemática - Resolução de 146 até 150](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/fD8ohgS6JKo/mqdefault.jpg)
![🔴 [ENEM 2025 PPL Live 02] Matemática - Resolução de 141 até 145](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/np7jAEKAjTE/mqdefault.jpg)
![🔴 [ENEM 2025 PPL Live 01] Matemática - Resolução de 136 até 140](/cdn-cgi/image/width=200,dpr=2,quality=85,format=auto,metadata=none,onerror=redirect/https://img.youtube.com/vi/vb1b6e7VXjw/mqdefault.jpg)
